近日,中國科學院上海硅酸鹽研究所科學家團隊在3D打印生物陶瓷用于骨、軟骨修復研究中取得系列進展。通過3D打印方法制備有序大孔結構的錳-磷酸三鈣(Mn-TCP)生物陶瓷支架,相關研究結果被《先進功能材料》(Advanced
Functional
Materials,adfm.201703117)接收,并申請專利一項。研究團隊與上海交通大學附屬第九人民醫院科研團隊合作,制備出了由空心管基元堆疊而成的3D打印生物陶瓷支架,相關研究成果發表在《生物材料》(Biomaterials,2017;
135: 85-95)上。同時,該研究小組還通過3D打印技術成功制備了硅酸三鈣骨水泥支架(ACS Appl Mater Interfaces.
2017;9(7):5757-5767) 及兼具抗菌與成骨活性的生物陶瓷支架 (Biofabrication.
2017;9(2):025037),在骨組織工程領域展示了良好的應用前景。
骨關節炎是一種退行性關節疾病,其臨床表現為關節的紅、腫、熱、痛、功能障礙及關節畸形,嚴重者導致關節殘疾、影響患者生活質量。關節炎疾病進程中,軟骨首先受到損傷,而軟骨損傷通常累及軟骨下骨,進而導致骨-軟骨缺損。由于軟骨和軟骨下骨的生物學特性不同,導致骨-軟骨一體化修復極具挑戰。研究團隊提出構建兼具軟骨-軟骨下骨一體化修復的3D打印生物陶瓷支架的策略,通過3D打印方法制備有序大孔結構的錳-磷酸三鈣(Mn-TCP)生物陶瓷支架。Mn的引入大幅度提高支架的致密度和抗壓強度。Mn-TCP生物陶瓷不僅可以通過激活HIF信號通路促進兔子軟骨細胞(Chondrocyte)和骨髓間充質干細胞(rBMSC)的增殖,支持軟骨細胞成熟和促進骨髓間充質干細胞向成骨分化,而且可以通過誘導炎癥模型的軟骨細胞產生自噬保護軟骨細胞。同時,體內修復實驗表明,Mn-TCP支架顯著促進軟骨下骨和軟骨組織的生成,在骨-軟骨一體化修復領域具有廣闊的應用前景。相關論文為(Advanced Functional Materials,adfm.201703117)。
研究團隊通過與上海交通大學附屬第九人民醫院科研團隊合作,在3D打印復雜仿生結構生物陶瓷用于血管化大塊骨缺損修復方面取得新進展。在臨床上,大塊骨缺損的修復一直是一個挑戰,由于3D打印技術可以便捷地制備形狀可控的多孔支架材料,而被廣泛應用于生物材料和骨組織工程領域。這種傳統的3D打印支架具有多孔的結構,將材料植入缺損部位后,營養物質和細胞會沿著孔向內滲入支架內部,進而有利于骨組織向內長入,最終促進骨缺損的修復。然而,傳統的3D打印支架在大塊骨缺損方面仍顯不足。第一,由于傳統的3D打印支架都是由實心的基元堆疊而成,這大大降低了材料的孔隙率;其次,傳統3D打印支架的孔隙呈階梯三維延伸狀,并沒有形成平直的通道狀,因此在流體力學上有較強的流體阻力,不利于營養物質和細胞滲入支架內部,從而阻礙了修復過程中的成血管和成骨。該研究組制備出由空心管基元堆疊而成的3D打印生物陶瓷支架。這種空心管結構的3D陶瓷支架比傳統的3D打印支架有更高的孔隙率。不僅能夠促進血管向內長入,同時還會促進干細胞和生長因子的傳遞更有利于大塊骨缺損的修復(Biomaterials,2017; 135: 85-95)。
相關研究工作得到了中組部青年千人計劃、科技部“863”計劃、國家重點研發計劃和國家自然基金的資助。

Mn-TCP生物陶瓷支架形貌表征圖,(A-C)TCP,(D-F)2.5 Mn-TCP,(G-I)5 Mn-TCP,(J-L)10 Mn-TCP。隨著Mn含量增加,支架的顏色逐漸由淺粉色變為深粉色,支架表面形貌也由TCP的多孔結構變為致密的液化形貌。
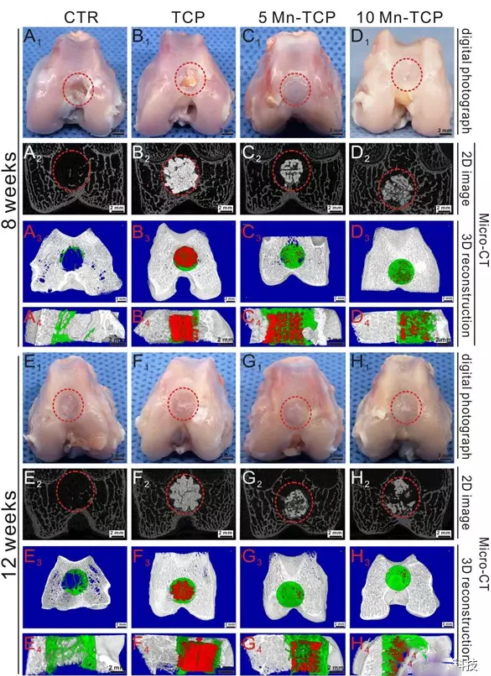
Mn-TCP生物陶瓷支架體內修復效果,A1-D4材料植入8周,(A1-4)空白對照組,(B1-4)TCP組,(C1-4)5 Mn-TCP組,(D1-4)10 Mn-TCP組;E1-H4材料植入12周,(E1-4)空白對照組,(F1-4)TCP組,(G1-4)5 Mn-TCP組,(H1-4)10 Mn-TCP組。Mn-TCP生物陶瓷支架組較空白對照組和TCP組顯著促進軟骨-軟骨下骨修復。
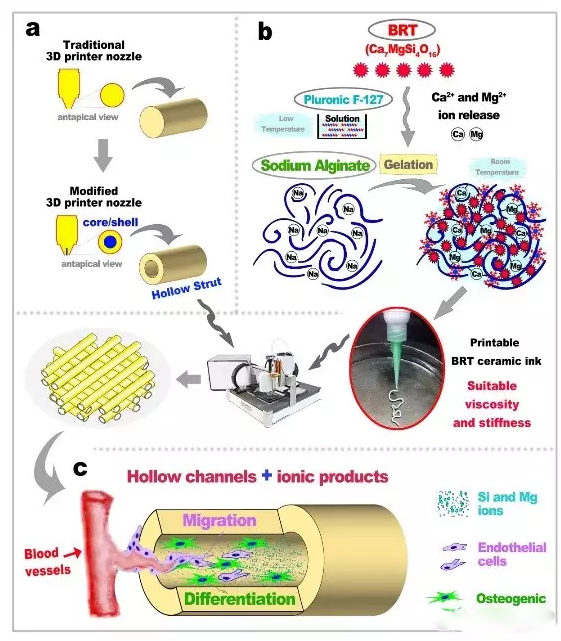
具有空心管復雜仿生結構的3D打印生物陶瓷支架用于大塊骨缺損的修復。

具有空心管復雜結構的3D打印生物陶瓷支架。
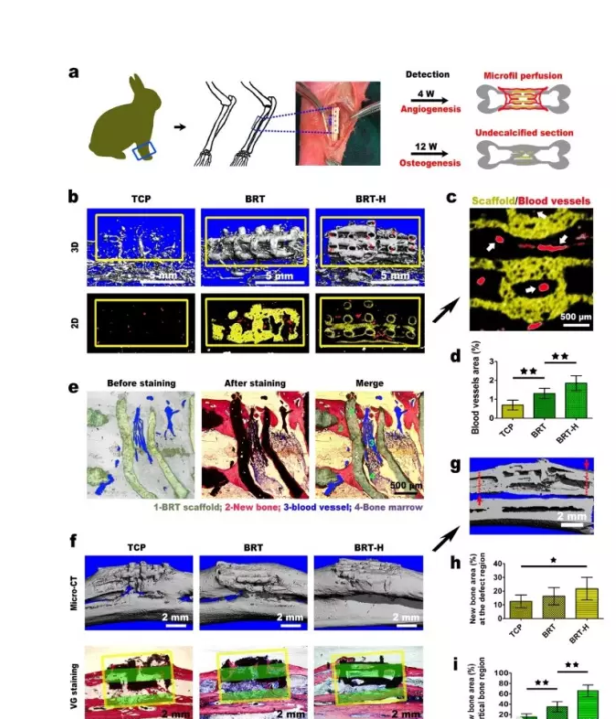
兔子大塊骨缺損修復實驗。實驗流程(a),體現成血管能力的micro-CT結果(b,c),體現成血管能力的組織學結果(d,e),體現成骨能力的micro-CT結果和組織學結果(g-i)。空心管生物陶瓷支架顯著誘導血管新生與大段骨缺損修復。